![]()
ドラッグディスカバリー支援技術:リガンド結合部位予測、構造ベースファーマコフォア予測
PIEFII Patent Right
- 世界初、化学第一原理のみに基づく究極のドラッグデザイン技術 -
これまでの構造ベース創薬を一新する世界初、次世代の革新ドラッグデザイン技術の開発に成功いたしました。これにより、創薬研究においてはリード探索、リード最適化、あるいは新薬開発に必要な時間と経費を極限まで短縮できるようになるだけでなく、その他の基礎研究分野においても未踏、最先端ツールとしてその威力を発揮することになるでしょう。
本革新技術は、Potential Interaction Energy Field with Interaction Informationの頭文字からPIEFIIと名付けられました。
PIEFII技術は生体高分子システム(タンパクや核酸、その他生体分子から成るシステム)の全体構造の原子座標情報のみから、本生体高分子(タンパク、核酸、糖)に特異的な外部因子であるリガンドや基質、あるいは金属原子や他の生体高分子が表面や内部で複合体を形成する相互作用部位(リガンド結合部位、基質結合部位など)を正確に予測することができるだけでなく、その相互作用部位で実際に複合体形成できる外部因子の骨格(スケルトンまたはスキャッフォルド)および化学的要求性(ファーマコフォア)を仮想的な外部因子の重原子位置に高精度に予測、視覚化します。
そのため、これまで医薬候補化合物の結合サイトやタンパク−タンパク相互作用部位が不明であるという理由により構造ベース創薬が不可能であった標的生体高分子に対しても、論理的な分子設計、薬物設計が可能となります。また、研究者は、生体高分子(タンパクや核酸)に複合体形成する天然の外部因子や医薬候補化合物などを経験と知識のみからしぼりこむことができるだけでなく、予測されたリガンド結合部位で直接低分子化合物を設計する、いわゆるデノボ(de Novo)デザイン、デノボ合成にも役立てることができます。さらに、ドラッグデザインなどの分子設計においては、得られたファーマコフォア情報をリード最適化などの構造修飾の方向性における指針として役立てることもできます。
予測に用いる生体高分子(タンパク、核酸、糖)の座標データは編集する等の特殊な作業を一切必要とせず、予測は標準的なサイズの生体高分子システムでも短時間で完了します。
構造ベース創薬の根幹をなす分子重ね合わせ技術に対する必須の基盤技術となるPIEFII技術は、Docking Study with HyperChemおよびVirtual Screening Systemに搭載されており、任意の化合物データベースから医薬候補化合物などを効率的に探索することを可能にしています。
図の説明
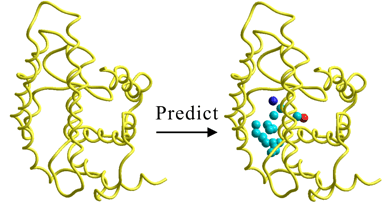
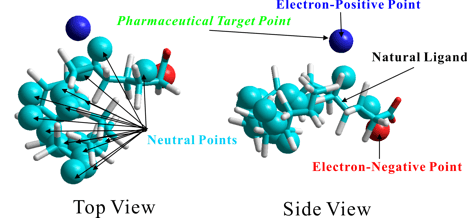
タンパク質分子における仮想相互作用相手の重原子位置を予測した結果を左図に示している。予測された重原子位置に、さらに予測された物理化学的性質をマッピングして実際のリガンドと同時に表示した結果を右図に示している。予測された重原子位置を含む部位が実際のリガンド結合部位と完全に一致しているだけでなく、予測された重原子位置を三次元的に結合して得られるスキャッフォルドが実際のリガンドのスケルトンを高精度に予測し、かつ各重原子位置の物理化学的性質が実際のリガンドの化学的特長を正確に予測している。特に、カルボキシル基に対応するファーマコフォアが正確に予測されている。さらに、図では実際のリガンドに占有されていない正電荷をもつ重原子位置が予測されており、この位置に向けてリガンドから置換基を導入することで親和性をさらに向上できることを示唆している。
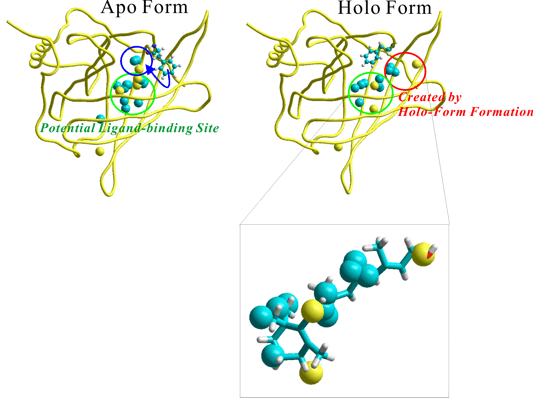
下の左図では、仮想相互作用相手の重原子位置予測をリガンドの結合していないアポ型に対して実施したものである。右図にリガンドと複合体を形成しているホロ型に対して予測したものを示す。これらの図から明らかなように、タンパク質自身で安定化しているアポ型においても潜在的な複合体形成部位を極めて正確に予測できることがわかる。また、アポ型からホロ型への変換に伴う内部構造の変化についても重要な示唆を与えている。つまり、アポ型におけるフェニルアラニン残基が予測された複合体形成部位上方の重原子位置に移動し、その結果新たに出現した相互作用部位と潜在的なリガンド結合部位が融合してホロ型における複合体形成部位(リガンド結合部位)を形成している。さらに、ホロ型においては、予測された重原子位置(ファーマコフォア)を含む部位が実際のリガンド結合部位と完全に一致しているだけでなく、予測された重原子位置を三次元的に結合して得られるスキャッフォルドが実際のリガンドのスケルトンを高精度に予測し、かつ各重原子位置の物理化学的性質が実際のリガンドの化学的特長を正確に予測している。また、ヨノン環下部に弱い負電荷の重原子位置が予測されており、この位置で酸化しているレチノール誘導体がリガンドになりうる可能性を示唆している。
その他のタンパク質(受容体)に対するリガンド結合部位予測結果も参照できます。
別酵素に対する基質結合部位予測結果についての客観的な意見について参照できます。
その他にもすでにご使用いただいているユーザー様からもPIEFII技術の革新性に対して大変ご興味いただいております。
本技術を用いた論理的ドラッグデザインのページが利用可能です。













